Une industrie chimique des algues en Bretagne
par Gérard Borvon et les élèves du lycée de l'Elorn à Landerneau.
Goémon, blé des vagues, pain de mer. Moisson qui lève sans semailles.
(Pierre Jakez Hélias)
Ce texte est le résultat d'une recherche à la fois historique et pédagogique menée avec des classes de seconde du lycée de Landerneau entre les années 1995 et 2000.
C'est un travail historique : il montre l'évolution et la permanence d'une industrie liée aux algues en Bretagne depuis le début du 18ème siècle.
C'est un travail pédagogique avec pour objectifs :
![]() de sortir l'enseignement des murs de l'école.
de sortir l'enseignement des murs de l'école.
![]() de faire participer les élèves à la construction de leur savoir.
de faire participer les élèves à la construction de leur savoir.
![]() d'étudier un programme dans le cadre d'un projet.
d'étudier un programme dans le cadre d'un projet.
![]() de situer une science et une technique, comme toute activité humaine, dans l'histoire et en particulier celle d'une région.
de situer une science et une technique, comme toute activité humaine, dans l'histoire et en particulier celle d'une région.
Vous y trouverez tous les dosages des éléments contenus dans les cendres d'algues. Les méthodes d'extraction de l'iode et des alginates. Les formules de masques de beauté et de moulages aux alginates. La recette d'un "flan" au "pioka". Le texte que nous présentons ici est une invitation à aller plus loin.

Le Nord-Finistère, en Bretagne, n'est pas particulièrement réputé pour son industrie chimique. Pourtant, depuis le 17e siècle, c'est à dire depuis le début de la chimie, une activité chimique y est menée, sans interruption, autour des algues.
L'industrie de la "soude" (carbonate de sodium) se développe d'abord. On extrait ce produit des cendres de goémons séchés. Il est indispensable à la fabrication du verre. Cette activité s'arrête à la fin du 18e siècle quand de nouveaux procédés sont découverts.
Elle reprend en 1829 après que le chimiste Bernard Courtois ait découvert, en 1812, un nouveau et utile produit dans les cendres d'algues : l'iode. L'iode est utilisée, en particulier, en photographie et en médecine. Sa production en Bretagne s'arrête en 1952 à cause de la concurrence de l'iode extrait des nitrates du Chili.
Aujourd'hui le relais est pris par l'extraction des alginates contenus dans les grandes laminaires.

En 1883 Edward Stanford isole l'algine des algues, plus tard le norvégien Axel Kefting en extrait l'acide alginique. La production à grande échelle commence en 1930. La Bretagne en produit environ 2000 tonnes dans les usines de Lannilis et Landerneau. Les alginates sont des agents épaississants et stabilisateurs qui interviennent aussi bien dans l'industrie pharmaceutique que dans l'industrie alimentaire ou celle du papier, des colorants ou des produits de moulage.
Plus confidentiels mais tout aussi riches d'intérêt sont les usages alimentaires, pharmaceutiques et cosmétiques des algues.De nombreux laboratoires, dans le Finistère, travaillent dans ces domaines pour des produits " haut de gamme " souvent destinés à l'exportation.
Cette ancienneté, cette richesse et cette diversité ont nourri les activités de plusieurs classes du lycée de l'Elorn à Landerneau. Ce site leur doit beaucoup. Il s'adresse à ceux qui voudraient s'inspirer de leur expérience mais aussi à tous ceux dont la curiosité aurait été éveillée par cette curieuse et attachante industrie.

En vous promenant sur les dunes du Nord-Finistère, vous ne pouvez manquer de rencontrer de longues tranchées tapissées de pierres plates. Les habitants du lieu vous dirons que ce sont les " fours à soude " des anciens goémoniers.
Pour le chimiste contemporain le mot " soude ", nom usuel de l'hydroxyde de sodium de formule NaOH, est déjà un archaïsme. La " soude " des goémoniers, quant à elle, évoque des temps encore plus reculés et désigne le carbonate de sodium (Na2C03). Dans un passé récent les droguistes savaient encore distinguer cette " soude du commerce " utilisée comme décapant banal de la " soude caustique " (l'hydroxyde de sodium) bien plus corrosive.
Un rapide coup d'œil dans un dictionnaire contemporain nous apprendra que le mot soude désigne également une plante des terrains salés appartenant à la famille des salsolacées qui comprend, entre autres, les salicornes. Le Larousse en trois volumes précisera même que le nom dérive de l'arabe " sunwäd ".
Ce sont bien les arabes qui ont introduit l'usage de la soude en Europe.
Depuis l'antiquité égyptienne, les populations du sud de la Méditerranée

Salicorne
savaient utiliser les propriétés des cendres des plantes terrestres riches en carbonate de potassium et celles des plantes marines contenant du carbonate de sodium. Le nom de " al kali ", par lequel les arabes désignaient ces plantes et leurs cendres, se retrouve dans le terme " alcalin " de la chimie récente. Ces cendres pouvaient être utilisées pour dégraisser les laines ou fabriquer des savons, elles entraient également dans la composition du verre.
Le verre, dont la découverte est attribuée aux égyptiens, est en effet un produit qui contient 70% de silice, 15% de chaux et 15% de soude ou de potasse.
Pour ceux que l'histoire du vocabulaire de la chimie intéresserait on peut signaler que, pour ces usages, les égyptiens de l'époque pharaonique utilisaient également les dépôts cristallins de carbonate de sodium déposés par évaporation sur les rivages des lacs Natron (Ouadi-Natroun), groupe de lacs à l'ouest du delta du Nil. Cette origine se retrouve dans le nom de natrium et le symbole Na retenus par la nomenclature internationale pour désigner ce que les chimistes français continuent à appeler sodium par référence à la soude.
On pourra noter également que le mot " kali " a donné le kalium de symbole K qui est le " potassium " de la nomenclature française. Cette autre exception française tire son nom du mot potasse, dérivé de l'allemand " Potasche " ou " Cendre de pot ". Ce terme a d'abord désigné le carbonate de potassium présent dans les cendres des végétaux terrestres et qui était utilisé, sous cette forme ou " lessivé " à travers un chiffon, pour la corvée de la " buée ", c'est à dire la " lessive " du linge sale. Le mot potasse désigne aujourd'hui l'hydroxyde de potassium.
Cette parenthèse étant refermée, il faut donc retenir que le carbonate de sodium extrait des cendres de plantes marines était une matière première indispensable aux industries du verre et du savon.
Aux 17e et 18e siècle la " pierre de soude " est un produit encore essentiellement importé d'Espagne. La soude d'Alicante est particulièrement réputée. Les arabes de l'époque andalouse ont introduit, dans cette région, la culture de la " Barille ", une variété de salicorne dont les cendres contiennent jusqu'à 30% de carbonate de sodium. Afin de rendre la France moins dépendante de ce pays parfois hostile, Colbert fera développer la culture de la salicorne et la fabrication de la " pierre de soude " sur les côtes françaises de la Méditerranée, inaugurant ainsi la vocation chimique de la région marseillaise.
La culture se fait sur les rives des étangs autour de Montpellier et Marseille. Les semailles sont faites en Février et Mars. La plante atteint la maturité fin Juillet, début Août, elle est alors jaune ou rouge et commence à sécher. On l'arrache, on la laisse faner comme le foin, on la bat avec des fléaux pour en recueillir la graine, elle est alors prête à être brûlée. Deux mille cinq cents quintaux d'herbes sèches donneront cent quintaux de " pierre de salicor ".
La combustion se fait dans une fosse circulaire de deux mètres cinquante de diamètre pour cinquante centimètres de profondeur tapissée de pierres. Le four est d'abord chauffé par des fagots de bois, la salicorne est ensuite jetée sur les braises en couches continues pendant trois heures environ. La cendre apparaît alors comme une masse en fusion qui est pétrie au moyen de perches de bois et qui deviendra un bloc compact lors du refroidissement. L'opération se poursuit jusqu'à ce que le fourneau soit rempli. Quand la " cuisson " de la pierre se fait de nuit on voit avec surprise dans la fournaise, une matière embrasée, liquide comme du métal fondu.
On ressent le même étonnement quand on observe l'aspect de lave en fusion de la soude des fours des goémoniers bretons au soir des démonstrations estivales.
/image%2F0561035%2F20240406%2Fob_33924d_four-a-goemon.jpg)
four de goémonier en Bretagne.
La salicorne pousse également sur les côtes bretonnes, normandes ou vendéennes. Pourtant c'est une matière première différente qui y sera à l'origine d'une industrie de la soude : le goémon. Les cendres de warech et de laminaires ont rapidement été utilisées comme substituts aux cendres de salicorne. Cependant leur réputation est mauvaise pour ce qui concerne le blanchissage et la savonnerie, elles sentent le " foie de soufre " (le sulfure d'hydrogène), elles dissolvent mal les graisses, elles tachent le linge. Par contre elles sont efficaces en verrerie.
A l'initiative de verriers installés dans la région de Cherbourg l'industrie de la " soude de warech " se développe donc en Normandie, en Bretagne et partiellement en Vendée. Le verre obtenu n'est pas un verre de qualité, les sels minéraux composant les algues le colorent en vert, mais c'est un " verre à bouteille " très utile à l'industrie vinicole française. L'activité ne se développe pas sans difficultés, il faut convaincre les pêcheurs inquiets pour la reproduction du poisson et rassurer les agriculteurs persuadés que les épaisses fumées des fours, à l'odeur âcre, viendront ruiner leurs cultures. De savants académiciens seront mobilisés et viendront sur place apporter la caution de la science.
/image%2F0561035%2F20240409%2Fob_5cf2c3_goemoniers-ile-vierge-mathurin-meheu.JPG)
Goémoniers devant l'Ile Vierge (Mathurin Méheut)
La technique des goémoniers est directement dérivée de celle des brûleurs de salicorne. Seule diffère la forme du four. La plus faible qualité combustible du goémon oblige à un four en tranchée orienté dans le sens des vents dominants. Les perches de bois utilisées pour malaxer la cendre en fusion cèdent la place à une perche de fer terminée par une pelle étroite : le " pifoun ". Le four est divisé en compartiments par des pierres transversales qui permettront un démoulage commode des " pains de soude " contrairement à la méthode méditerranéenne qui oblige à casser la " galette " en morceaux irréguliers.
L'une des premières industries chimiques développée en France s'est donc installée en Bretagne. La transformation des algues est, depuis cette date, restée la seule activité chimique consistante de cette région. L'industrie de la soude, pour sa part, s'y maintiendra jusqu'à la fin du 18e siècle.
Très tôt, les chimistes avaient su reconnaître que la soude de warech contenait un élément présent dans le sel marin. L'idée de fabriquer la soude à partir de ce sel était donc naturelle. Elle ne se concrétisera qu'à la fin du 18e siècle. En 1781, l'Académie des sciences lance un concours pour " trouver le procédé le plus simple et le plus économique " de fabriquer de la soude à partir du sel marin.
Voir à ce sujet le mémoire présenté par Lavoisier
Deux propositions retiennent l'attention de l'Académie. L'une faite par un chimiste alsacien nommé Hollenweger, l'autre par Guyton de Morveau chimiste bourguignon déjà renommé. Les deux lauréats sont invités à rechercher une région exempte de gabelle pour y installer une manufacture. Tous les deux se retrouvent en Bretagne. L'un, Guyton de Morveau, s'installe au Croizic, l'autre, Hollenweger, au Pouliguen. Cependant, aucun de ces deux manufacturiers n'a vraiment réussi à développer sa méthode au moment où le Comité de Salut Public de la République lance un appel à tous les savants pour qu'ils établissent un procédé vraiment efficace.
Celui de Nicolas le Blanc est retenu. Il consiste à faire agir de l'acide sulfurique sur le chlorure de sodium dans une chambre en plomb. Le sulfate de sodium obtenu est ensuite porté à haute température en présence de charbon et de calcaire. Le chimiste moderne traduirait ces deux réactions par les équations suivantes :
H2SO4 + 2 NaCl -> Na2SO4 + 2 HCl
Na2SO4 + 2 C + CaCO3 -> Na2CO3 + CaS + 2 CO2
Pendant un siècle ce procédé restera le seul utilisé par l'industrie mais celle-ci ne s'installera pas en Bretagne. Depuis l'abolition des privilèges le sel breton a le même prix que celui des autres régions et rien ne pousse plus les industriels à venir s'installer dans cette province excentrée.
Quant à la soude de warech, autant ne pas en parler, elle n'a aucune compétitivité par rapport à la soude dite " factice ". Le métier de " soudier " aurait donc dû disparaître en Bretagne, si un événement fortuit ne l'avait pas relancé sur une autre base. Nous en reparlerons.
Depuis plusieurs années, les populations du Nord-Finistère ont voulu faire revivre la tradition du métier de goémonier. A Plouguerneau, un musée a choisi d'en conserver les outils et les gestes. Chaque été, ici ou là, les fours sont remis en activité pour une fête qui n'attire pas uniquement les touristes.
Professeur de physique-chimie au lycée de l'Elorn à Landerneau, attaché à la région de Lilia-Plouguerneau et au métier de goémonier par tradition familiale, j'ai eu, très tôt, le sentiment que les cendres d'algues, et les algues elles-mêmes, pourraient constituer un produit de choix pour la construction d'un cours de chimie.
Petit à petit ce sentiment s'est transformé en une pratique. Des élèves ont procédé au brûlage des algues sous la conduite des derniers représentants de la profession qui faisaient revivre les tours de main ainsi que le vocabulaire, en breton, du vieux métier. Les cendres ont été concassées, tamisées, analysées et dosées au laboratoire. La chimie y trouvait une couleur nouvelle, plus chaleureuse, plus humaine, reliée à une histoire proche, sans que pour autant le " programme " soit oublié.
Mais pourquoi ne voir que le passé ?
L'activité chimique autour des algues est, plus que jamais vivante en Bretagne. Les laminaires sont une source essentielle pour les alginates dont les domaines d'utilisation croissent sans arrêt. L'industrie alimentaire, cosmétique et pharmaceutique exploitent de plus en plus les ressources des plantes marines dans lesquelles on découvre en permanence de nouvelles propriétés.
Les " goémoniers" d'aujourd'hui sont des marins équipés de moyens modernes de récolte. Ce sont également des ingénieurs et des techniciens de haut niveau qui pratiquent dans des laboratoires ou des unités de production à taille humaine une " chimie du vivant " qui a de quoi séduire. Nous leur avons rendu visite. Ils nous ont initié à une chimie qui ne se trouve pas dans nos livres scolaires. Ils nous ont confié l'essai de leurs produits. Nous avons adapté leurs techniques à nos salles de travaux pratiques et constaté, là encore, que nos programmes de chimie " organique " pouvaient très bien se construire autour des algues.
Par séquences séparées, mais aussi parfois dans le cadre d'un projet construit sur l'ensemble de l'année scolaire, les algues, d'hier et d'aujourd'hui, sont donc entrées dans nos classes. Ce sont des éléments de ces travaux que nous proposons ici. L'année 2000 verra l'introduction dans les classes de seconde des lycées, de thèmes et de méthodes très proches de ce que nous avons réalisé. Des enseignants y trouveront peut-être des idées. Des élèves pourront y trouver des pistes pour des travaux personnalisés. Des apprentis chimistes voudront peut-être en reproduire certaines manipulations qui peuvent se faire, chez soi, avec peu de matériel.
Nous destinons également ce texte, qui est un travail de mémoire, à tous ceux que cette tradition, qui a fait se côtoyer des marins, des manufacturiers et des chimistes, intéresse. Au delà des techniques et des formules, c'est la vie d'une région qui est concentrée dans cette chimie.
Pour reprendre l'expression d'un élève d'une classe de seconde :
" ici des hommes ont su extraire de la nature, en la respectant, le mieux de ce qu'elle pouvait offrir ".
________________________________________________
Extraction de la soude (carbonate de sodium)
Le musée des goémoniers à Plouguerneau, sur la côte du Nord-Finistère, organise chaque été un brûlage des algues dans les anciens fours afin d'obtenir les cendres riches en soude.
Nous nous sommes rendus sur place pour extraire un " pain de soude " qui se présente sous une forme très compacte. Les cendres chaudes ont un aspect de matière en fusion et se moulent dans les alvéoles du four pendant leur refroidissement.
On peut également réaliser la combustion d'algues sèches dans une fosse de 40 à 50 cm de côté creusée dans le sol et tapissée de pierres plates.
Le traitement au lycée.

Le travail au pifoun dans le four.

Concasser le pain de soude

opération de lessivage

analyser le filtrat
La découverte de l'iode est due au chimiste Bernard Courtois (1777-1838). Fils d'un maître salpêtrier de Dijon, il reprend cette activité à Paris au moment où les guerres de Napoléon réclament le salpêtre nécessaire à la fabrication de la poudre à canons. En tant que responsable de la régie des poudres, Lavoisier a donné à cette activité une nouvelle rationalité. Le salpêtre est élaboré dans des « salpêtrières » où le développement des bactéries nitrifiantes sur des mélanges terreux appropriés est favorisé. Les terres enrichies en salpêtre doivent alors être lessivées. Les eaux-mères obtenues sont ensuite traitées par des cendres de bois riches en potasse afin d'obtenir la cristallisation du salpêtre.
Cependant le blocus commercial organisé autour de la France rend difficile l'approvisionnement en cendres potassiques dont la Suède est le principal fournisseur. Courtois tente donc l'essai des cendres de warech. Ces dernières contenant des composés sulfurés indésirables, le chimiste entreprend de décomposer ceux ci par l'acide sulfurique concentré. C'est à cette occasion qu'il observe le dégagement de vapeurs violettes et la précipitation d'un corps noir et brillant. Courtois est un chimiste suffisamment avisé pour comprendre qu'il est en présence d'un corps nouveau. Il en prépare une petite quantité qu'il confie à ses amis Clément et Désormes pour en faire une étude chimique qui sera ultérieurement complétée par Gay-Lussac et Davy. Cette découverte est annoncée à l'Académie des Sciences le 29 Novembre 1813 par Nicolas Clément. Le mot grec iôdês (violet) inspire le nom de « iode » qui est donné à ce produit par référence à la couleur de ses vapeurs.
Rapidement l'iode apparaît comme un produit de grand intérêt. Il est à l'origine des premiers daguerréotypes, photographies sur plaques de cuivre argentées sensibilisées aux vapeurs d'iode. C'est, en solution dans l'eau ou l'alcool, un excellent désinfectant encore très utilisé aujourd'hui. On reconnaît également, très vite, son efficacité contre le goitre. C'est donc un produit précieux dont la production s'annonce rémunératrice.
En 1828, arrive en Bretagne un jeune chimiste prêt à tenter l'aventure de sa production industrielle. François-Benoît Tissier a d'abord dirigé, à Paris, l'usine d'iode crée par son professeur, le chimiste Clément. Il y met au point une méthode efficace. Au Conquet, il rencontre la famille Guilhem déjà engagée dans cette aventure mais sans grande conviction. Il leur rachète leur fabrique et commence alors une ère de prospérité qui permettra à Tissier d'amasser une fortune colossale.
Le succès amène des concurrents. Des usines s'ouvrent à Granville (1832), Pont-Labbé (1852), Vannes (1853), Quiberon, Portsall (1857), Tréguier (1864), L'Aber-Wrach (1870), Guipavas (1877), Lampaul-Plouarzel, Audierne (1895), Loctudy, Penmarc'h (1914), Plouescat, Argenton (1918). Toutes ne connaîtrons pas le succès, d'autant plus qu'une rude concurrence existe avec l'iode du Chili.
Dès 1830 on constate que les riches gisements de nitrates du Chili contiennent de l'iode. Abondant, facile à extraire, il pourrait inonder les marchés européens si des mesures protectionnistes n'étaient pas prises. Un organisme international la « combinaison de l'iode » fixe la part de marché de chaque usine et le cours de l'iode. Le Chili qui pourrait produire jusqu'à 3000 tonnes par an limite sa production à 900 tonnes. L'Angleterre et la France disposent chacune d'un quota de 70 tonnes. Cet accord permet à l'industrie française de se maintenir jusqu'à 1955 environ. A cette date le gouvernement français décide de lever les mesures protectionnistes et invite les manufacturiers à rechercher un autre débouché pour les algues. S'ouvre alors l'ère des alginates.
L'iode est extrait des cendres d'algues, le vieux métier de producteur de soude se poursuit donc avec la nouvelle activité. Un problème cependant : pour obtenir de beaux pains de soude, bien gris et bien compacts, il fallait des températures élevées et une combustion vive. A l'inverse la production d'iode nécessitait une température modérée, les iodures étant des corps très volatils. Plusieurs brevets avaient été déposés pour des fours à combustion ménagée utilisant la chaleur produite afin de sécher les algues mais aucun ne débouchera sur des applications rentables. Il aurait fallu pour cela pouvoir dépasser le maigre quota de production attribué à la France. Les goémoniers reprendront donc les vieux fours de leurs pères. Ils voudront, comme eux, mouler de beaux pains de soude en faisant brûler les algues à feu vif au détriment de la teneur en iode des cendres et ceci malgré la pression exercée par les manufacturiers qui les payaient en fonction de cette teneur. Il est vrai que des pains bien compacts se transportaient mieux, surtout si on devait les ramener des îles où les goémoniers faisaient de longues campagnes.
La teneur en iode dans les algues séchées variait suivant les algues de 2% à 3%. Dans les cendres cette teneur tombait de 1% à 1,5%. Reste à extraire cet iode.
Lixivation : Les cendres sont concassées en morceaux de l'ordre de quelques cm 3. Le broyage se fait à la masse sur une table recouverte d'un plaque de fonte. Le lessivage dégage une partie soluble qui peut représenter jusqu'à 65% de la totalité. Les lessives contiennent de 6kg à 9kg d'iode au m3.
Concentration : Les solutions sont concentrées par évaporation dans des chaudières peu profondes chauffées à feu nu ou encore en utilisant des serpentins où circule de la vapeur d'eau sous pression. Le chlorure de sodium se dépose d'abord, le chlorure de potassium ensuite. Les eaux mères finales contiennent 100g à 150g d'iode par litre mais aussi les carbonates, les sulfures, sulfites et hyposulfites solubles.
Désulfuration : La désulfuration se fait en milieu acidifié. Il faut verser de l'acide sulfurique ou de l'acide chlorhydrique dans la solution qui à l'origine est très basique. Les carbonates se décomposent les premiers avec un dégagement de dioxyde de carbone. Les composés sulfurés se décomposent ensuite avec un dégagement de sulfure d'hydrogène et un précipité de soufre sous forme essentiellement colloïdale. En portant la solution à ébullition on chasse le sulfure d'hydrogène dissout et on favorise la précipitation du soufre.
Précipitation de l'iode : L'iode est chassé de la solution par l'action du chlore. Celui ci est obtenu par l'addition de chlorates dans la solution acide (au laboratoire on pourra utiliser de l'eau oxygénée). L'iode se précipite alors sous la forme d'une poudre noire.
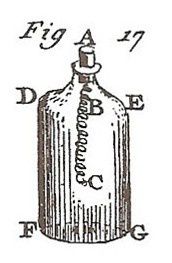
Sublimation : L'iode lavé et séché par pression est sublimé dans des cuves de céramique surmontées d'un couvercle sous forme de cloche chauffées sur bain de sable. On obtient alors des paillettes contenant de 97% à 98% d'iode. Une nouvelle sublimation peut porter ce taux à 99,5%. C'est en nous inspirant de ces techniques que nous procéderont à l'extraction de l'iode puis à son dosage.

Vapeurs d'iode violettes.
Nous avons extrait l'iode de la solution par action de l'eau oxygénée H2O2 en milieu acide.
| Etapes de la manipulation | Réactifs et méthodes utilisés | observation |
|---|---|---|
| Acidification de la solution | Acide sulfurique concentré | L'acidification de la solution a pour premier effet de libérer le dioxyde de carbone provenant des ions carbonates |
| Libération de l'iode | eau oxygénée | L'eau oxygénée oxyde les ions iodure, il se forme de l'iode qui colore la solution en brun. On observe même un léger précipité d'iode. |
| mise en évidence de l'iode gazeux | chauffage | Un chauffage léger libère les vapeurs d'iode violettes |
Aujourd'hui - Les alginates et les carraghénanes
L'anglais Edward Stanford (1837-1899) isole, dans les algues, un gel qu'il désigne du nom d'algine. Le norvégien Axel Krefting est le premier à en extraire l'acide alginique. Ce produit trouve un intérêt immédiat comme apprêt pour les tissus. Sa production à grande échelle commence vers 1929 sur les côtes californiennes.
En Bretagne, cette industrie débute à Pleubian, dans les Côtes d'Armor, dès le début du siècle. Elle ne prendra son essor que vers les années 1960. A cette date l'état français a décidé de ne plus subventionner la fabrication de l'iode, obligeant ainsi les manufacturiers à se reconvertir. Ceux-ci font preuve d'une extraordinaire capacité d'adaptation. Il faut d'abord élaborer la théorie de l'extraction, il faut inventer et construire de nouvelles machines. Il faut surtout imaginer les utilisations possibles d'un produit aux débouchés encore limités.
Beaucoup d'usines disparaissent dans la tourmente mais le pari est gagné et le Nord-Finistère devient le producteur principal de l'alginate en Europe. Actuellement de l'ordre de 2000 tonnes par an sont produites dans les deux usines de Lannilis et de Landerneau qui se partagent le marché. L'essentiel de la production est exporté mais, sur place, une constellation de petites entreprises utilisent cette matière première pour des produits cosmétiques, pharmaceutiques ou alimentaires.
L'alginate est utilisé comme épaississant et stabilisateur dans les glaces, les crèmes et même les yaourts et les fromages frais. Dans la nomenclature européenne ce sont les E 400 et E 411. On trouve encore les alginates dans la fabrication du papier, de la peinture, des électrodes....Un marché en constante expansion qui n'est limité que par la quantité d'algues que l'on peut récolter. En Bretagne cette quantité est limitée aussi la production est-elle orientée vers des produits de qualité destinés aux industries cosmétiques, pharmaceutiques et alimentaires.
Depuis plusieurs siècles le Chondrus est une algue utilisée en médecine et dans l'alimentation. Il y a plus de 600 ans les irlandais du comté de Carragheen dans le sud de l'Irlande savaient utiliser cette " Irish moss " pour des pommades et des flans. Cette algue séchée a, en effet, un extraordinaire pouvoir gélifiant en présence de lait. Les émigrants irlandais ont emporté leurs recettes avec eux quand, vers 1700, ils ont rejoint l'Amérique du Nord et constaté que leur " irish moss " poussait également sur les côtes du Massachusetts. Le polysaccharide extrait de cette algue et obtenu pur vers 1871 a été logiquement nommé carrageenan dans la nomenclature de la Société Chimique Américaine et est encore désigné sous ce nom.
En Bretagne, le Chondus Crispus est également abondant. Dans le Léon finistérien on le désigne par le terme de " pioka ", en Cornouailles il est parfois appelé " piko ". Une tradition de gâteaux et flans au pioka existe dans le Nord-Finistère. Est-elle ancienne ? Il est certain, par contre, que dès le début du 19ème siècle les industriels on su mesurer l'intérêt de ce produit. La cueillette du pioka, les jours de grande marée, est devenue une activité rémunératrice qui se pratique, encore de nos jours, avec les mêmes méthodes. Jadis vendu sec et blanchi, il est acheté humide aujourd'hui, sauf pour de petites productions artisanales. Actuellement, une seule usine, installée en Normandie, produit les quelques 3000 tonnes fabriquées en France.
Comme les alginates, les carraghénanes sont utiles dans l'industrie textile, la peausserie, la fabrication des peintures. Le gel qu'ils forment avec le lait les font utiliser en priorité dans tous les produits alimentaires lactés, mais aussi dans les bières, les pâtes alimentaires, les confitures.
Deux entreprises d'alginates à Landerneau
Dans la région de Landerneau, deux entreprises traitent les algues pour en utiliser les alginates.
L'entreprise Danisco est spécialisée dans l'extraction de l'acide alginique à partir des algues brutes.
L'entreprise Technature utilise les alginates pour élaborer des produits finis.
L'entreprise Danisco : Nous l'avons visitée sous la direction de son directeur Monsieur Pasquier. L'usine (9000 mètres carrés d'ateliers et de laboratoires) traite chaque année 6000 tonnes d'algues séchées pour la production d'alginates particulièrement purs utilisés pour la pharmacie et l'alimentation. La société Danisco nous a fourni un sachet d'acide alginique pur pour en étudier les propriétés. Son directeur nous a également détaillé le procédé d'extraction des alginates à partir des algues (voir fiche).
L'entreprise Technature : Nous y avons été reçus par son directeur, Monsieur Le Fur, et par son directeur commercial, Monsieur Winkler (aujourd'hui directeur de l'entreprise Lessonia). L'entreprise conditionne les alginates pour ses différents usages : moulages, cosmétiques, alimentation... Sa clientèle est mondiale (Europe, U.S.A, Japon). La réputation des produits bretons est internationale ! L'entreprise nous a confié des alginates de moulage pour que nous puissions réaliser un moulage. Elle nous a également proposé de mettre au point un nouveau masque de beauté.
Nous y avons extrait les alginates contenues dans des laminaires. Nous avons utilisé pour cette manipulation des laminaires de l'espèce " laminaria digitata " dont le nom en langue bretonne est " tali ".
Les procédés d'extraction des alginates nous ont été expliqués par M. Pasquier directeur de l'usine DANISCO et M. Le Fur directeur de l'entreprise TECHNATURE. Nous avons réalisé cette opération en suivant les étapes indiquées dans le tableau ci-dessous. Nous avons utilisé pour cette manipulation des laminaires de l'espèce " laminaria digitata " dont le nom en langue bretonne est " tali ".
| Nature de l'opération | méthode | observation |
|---|---|---|
| préparation des algues | découper une algue fraîche (laminaire) en morceaux (1cm x 1cm) ou réhydrater des morceaux d'algue sèche. | Il faut utiliser des algues fraîches ou rapidement séchées après la cueillette. |
| Déminéralisation | faire " mariner " les algues dans trois bains successifs de 25 minutes chacun d'une solution d'acide sulfurique à pH=2 | Les algues prennent une consistance très ferme. Le bain d'acide dissout les sels minéraux et prend une coloration verdâtre. |
| Formation de l'alginate de sodium soluble | les algues sont placées dans une solution de carbonate de sodium à pH=11. | Les morceaux d'algues se ramollissent, l'ensemble prend un aspect pâteux dû à la dissolution de l'alginate de sodium. |
| Filtration, blanchiment | La pâte est pressée à travers un tissu de coton blanc afin de séparer l'alginate de la cellulose | le filtrat obtenu est légèrement gélatineux et faiblement coloré. On peut le décolorer par quelques gouttes d'eau de Javel (hypochlorite de sodium) |
| précipitation de l'acide alginique | On utilise une solution d'acide sulfurique ou d'acide chlorhydrique. | Il faut atteindre un pH=1,8 l'acide alginique se coagule. On peut l'extraire en utilisant un agitateur ou en filtrant. |
Nous avons également construit des modèles moléculaires de ces monomères et de leurs polymères.


L'alginate de moulage est une poudre blanche composée d'alginate de calcium et de terre de diatomée (contrairement à l'alginate de sodium qui est soluble dans l'eau, l'alginate de calcium forme un gel insoluble). Mélangée à quatre fois son poids d'eau, la poudre d'alginate se transforme en une pâte onctueuse. Elle gélifie en 6 à 10 minutes en fonction de la température et de la concentration. On obtient une masse souple et résistante qui permet de réaliser le moule dans lequel on viendra verser du plâtre ou de la cire. Sa rapidité de prise, sa finesse de reproduction, son absence totale d'agression, en font un matériau idéal pour mouler des objets vivants : une main, le pieds d'un bébé, un visage.
Préparation de la pâte :
prévoir 300g de poudre pour un litre d'eau. Verser l'eau sur la poudre et mélanger activement avec une main pendant une minute pour obtenir une pâte homogène. A partir de ce moment on dispose d'un temps de travail de 3 à 5 minutes pour réaliser le moule. Ce moule dans certains cas pourra être utilisé deux ou trois fois si le démoulage ne l'a pas endommagé.
Que mouler ?
De façon classique on peut démarrer par la trace d'un animal sur le sol. La rapidité de la prise et la finesse de l'empreinte sont immédiatement perceptibles. La contre-empreinte réalisée en plâtre sera riche de détails.
Le plus spectaculaire : le moulage d'une main d'enfant !
Il faut trouver un pot pas trop large mais dans lequel la main de l'enfant puisse plonger jusqu'au dessus du poignet. Faire un essai du volume de pâte de moulage nécessaire en remplissant d'eau le récipient dans lequel l'enfant a plongé sa main. Calculer la quantité de poudre nécessaire ( ¼ du poids de l'eau).
Préparer la pâte. Verser la pâte dans le coffrage.
Masser la main avec un peu de pâte, celle ci ne collera pas à la peau en durcissant mais vous obtiendrez ainsi de fins détails.
Plonger la main dans le coffrage jusqu'à ce que les doigts touchent le fond et remonter légèrement.
Maintenir la pause quelques minutes, on sentira alors que l'alginate est bien gélifié, il résistera sous la pression des doigts et se détachera bien de la peau. Un petit tour de main pour décoller le moule : agiter les doigts doucement en rapprochant le pouce du petit doigt.
L'enfant doit, de la sorte, retirer la main sans trop de difficultés.
Un conseil : la surface de l'alginate est légèrement acide, le plâtre de moulage prend mal à son contact. On peut y remédier en versant dans l'empreinte une solution diluée de bicarbonate de sodium pour la rincer rapidement.
L'entreprise Technature nous a confié la mise au point d'un masque de beauté. C'est un nouveau produit que l'entreprise souhaite commercialiser. Il s'agit d'un masque aux fruits tropicaux dont le support est constitué par un alginate de moulage.
Nous avons testé un premier masque d'alginate sans aucun additif afin d'observer l'effet " moulant " de ce produit. Nous avons ensuite essayé plusieurs formulations en faisant en particulier varier les colorants et les parfums. Pour finir, nous avons testé le masque obtenu

préparation phase 1
La recette d'un masque de beauté
alginates
couleur naturelle
extrait de papaye, d'ananas

phase 2
Dose : 30g de poudre d'alginate pour 100g d'eau.
Dilution du produit
Verser rapidement l'eau sur la poudre. Mélanger énergiquement jusqu'à l'obtention d'une pâte lisse et onctueuse. Important : La dilution se fait dans de l'eau à 20°C.
Application
Appliquer immédiatement sur le visage en évitant le contour des yeux. La prise a lieu au bout de 6 minutes.
Durée du soin 15 minutes environ.
Résultat peau plus douce plus fine, teint plus lumineux

Réalisation du masque.
__________________________________________________________________________________
Agar-Agar est un mot malais.
Ce corps, utilisé en Malaisie, était également d'un usage courant au Japon et dans tout l'Extrême-Orient. L'Agar-Agar provient d'algues diverses et en particulier de l'espèce gélidium. Ces algues, après des lavages fréquents, sont séchées et soumises à ébullition. Le gel obtenu est déshydraté puis réduit en poudre.
Le pouvoir gélifiant de l'Agar-Agar est extrême. Deux grammes dans un quart de litre d'eau portée à ébullition pendant 5 minutes donnent un gel très ferme après refroidissement.
Au laboratoire de biologie, l'Agar-Agar sert à préparer des supports nutritifs pour les plantes. Au laboratoire de chimie, il sert, par exemple, à préparer des " ponts électrolytiques " conducteurs dans l'étude des piles.
Nous avons préparé un gel d'Agar-Agar coloré par de l'hélianthine. L'Agar-Agar est aussi utilisé pour préparer des flans mais nous avons utilisé pour cela une algue originaire de Bretagne, le Pioka, qui contient des carraghénanes.

_________________________________________________________________________________

pioka de Bretagne
Pioka est le nom breton d'une algue qu'on appelle également " lichen " de mer. On la récolte aux grandes marées, son prix élevé attire les cueilleurs saisonniers. Son nom scientifique est Chondrus crispus. Le principe actif qu'on en extrait est constitué par les carraghénanes . C'est un excellent gélifiant dans le lait. De façon traditionnelle, il est utilisé par les populations côtières du Nord de la Bretagne pour réaliser des " flans ". Préparation des algues Après la récolte, les algues sont étalées sur les dunes et séchées en les retournant fréquemment. On peut également les arroser d'eau douce de temps en temps afin de les débarrasser du sel et des débris divers. A la fin de ce traitement les algues sont blanches et sèches on peut alors les conserver. Juste avant l'usage On peut parfaire le rinçage par trempage et rinçages répétés. Les algues doivent être totalement débarrassées de leur odeur de " mer "
Recette de flan au pioka
Nous avons réalisé la recette de dessert suivante. Elle nous a été communiquée par une personne agée de la région de Brignogan dans le Nord-Finistère. Elle l'avait vue elle même réalisée par ses parents.
Remarque : les carraghénanes du pioka donnent facilement un gel avec le lait, il ne donnent pas de gel avec de l'eau. Pour cela il faudrait utiliser de l'Agar-agar que nous avons également testé (il est également utilisé pour des flans).
Utiliser une petite poignée d'algues sèches par quart de litre de lait. Les rincer. Faire bouillir pendant 5 à 10 minutes dans le lait en remuant. Filtrer le lait chaud dans une passoire ou une écumoire. Remettre le lait à bouillir cinq minutes avec l'arôme souhaité, chocolat ou vanille sucrés ( par exemple 3 cuillérées de Nesquik par ¼ de litre de lait). Verser dans des coupes. Laisser refroidir et mettre au frigo.


Si, comme nous, vous ignoriez que la chimie, depuis si longtemps, s'intéressait aux algues, vous savez maintenant que, chez nous en Bretagne, des personnes ont fabriqué, et fabriquent encore, des produits utilisés dans le monde entier.
Nous avons rencontré des " anciens ". Goémoniers et manufacturiers. Ils nous ont transmis la fierté qu'ils gardent de leur métier. Nous avons, également, rencontré les acteurs modernes de cette aventure. Des marins qui font un travail toujours hasardeux mais qui ont mis au point des techniques sures et efficaces et ne vivent plus la vie de forçats de leurs ancêtres exilés sur les îles. Des chimistes extrayant de la nature le meilleur de ce qu'elle peut fournir. Des biologistes mariant les essences et les extraits pour embellir, soigner ou nourrir.
Pour ce qui est de notre programme scolaire, il a avancé sans que nous nous en rendions compte. Etude théorique, recherche documentaire, visite des usines et discussion avec les chimistes de métier, manipulations au laboratoire, mise au point de nouvelles recettes et de nouveaux produits...tout cela faisait partie du même projet.
En rédigeant ce dossier nous avons eu le désir de garder la trace de notre travail et de transmettre cette expérience à tous ceux qui voudraient la partager et la compléter. Nous avons également pensé à nos lecteurs et lectrices qui ne seraient ni chimistes ni lycéennes ou lycéens . Nous avons cherché à leur faire découvrir un aspect de l'histoire et de l'actualité de notre région. A elles et eux de nous dire si l'objectif a été atteint.
La classe de seconde A, année 1997/1998, La classe de seconde C, année 1998/1999 et leur professeur, Gérard Borvon
Une suite à notre travail
Second prix du concours CEFIC pour l'enseignement des sciences.
Ce travail a reçu le second prix européen au concours CEFIC de 1999.
Il est cité et en partie repris sur le site CultureSciences-Chimie de l'école normale supérieure de Cachan.
voir : Les algues : une « agroressource » d'avenir
Il a fait également l'objet d'un sujet à des olympiades de chimie.

Une reconnaissance de la place historique de la Bretagne dans l'étude et l'industrie des algues.
/image%2F0561035%2F20230825%2Fob_97e52b_algues-congres.png)
/image%2F0561035%2F20230825%2Fob_1df808_algues-recolte.jpg)
Et pour terminer en chansons
/image%2F0561035%2F20230825%2Fob_c293a0_storlok-algues.JPG)
Ecouter :
Storlok - Gwerz ar vezhinerien
Un livre.
/image%2F0561035%2F20231001%2Fob_1bcfe6_l-or-brun-des-faucheurs-de-la-mer.jpg)
Les champs d’algues entre Quiberon au sud et la côte d’Émeraude au nord sont exceptionnels. Ils ont permis diverses pratiques et usages qui ont pris de l’ampleur avec la production de l’iode et l’utilisation de l’engrais. Depuis les années du romantisme jusqu’à celles de l’abstraction, plus de 120 peintres ont trouvé leur inspiration dans ce thème jusqu’alors inédit.
_______________________________________________________________________________________
Deux poèmes de Pierre Jakez Hélias
(qui a été mon professeur à l'Ecole Normale d'Instituteurs de Quimper.)
/image%2F0561035%2F20240406%2Fob_5dbd18_numerisation-20240406-4.jpg)
/image%2F0561035%2F20240406%2Fob_39279d_numerisation-20240406-3.jpg)














/image%2F0561035%2F20140324%2Fob_6b7b8e_003-vinci-dodecaedre-02.jpg)